Zákony termodynamiky: Základní principy tepelné energie
Úvod do termodynamiky
Zákony termodynamiky tvoří základní pilíře naší znalosti o tepelné energii a jejím chování. Tyto fundamentální principy popisují, jak energie proudí, transformuje se a interaguje s hmotou. Pochopení zákonů termodynamiky je klíčové nejen pro vědce a inženýry, ale i pro běžné lidi, neboť ovlivňují každodenní jevy kolem nás.
První zákon termodynamiky: Zákon zachování energie
První zákon termodynamiky, známý také jako zákon zachování energie, stanoví, že energie nemůže být vytvořena ani zničena, pouze přeměněna z jedné formy na jinou. Tento princip má zásadní význam pro pochopení energetických přeměn v přírodě i technologiích.
Matematické vyjádření prvního zákona
Matematicky lze první zákon termodynamiky vyjádřit rovnicí:
CopyΔU = Q – W
Kde:
- ΔU je změna vnitřní energie systému
- Q je teplo dodané do systému
- W je práce vykonaná systémem
Tato rovnice popisuje, že změna vnitřní energie systému je rovna rozdílu mezi teplem dodaným do systému a prací vykonanou systémem.
Praktické příklady prvního zákona
- Vaření vody: Při ohřevu vody na sporáku se elektrická energie mění na tepelnou, která zvyšuje teplotu vody.
- Fotosyntéza: Rostliny přeměňují sluneční energii na chemickou energii uloženou v glukóze.
- Dobíjení baterie: Elektrická energie se ukládá jako chemická energie v baterii.
- Brzdění auta: Kinetická energie vozidla se mění na tepelnou energii v brzdových destičkách.
- Svítící žárovka: Elektrická energie se přeměňuje na světelnou a tepelnou energii.
Druhý zákon termodynamiky: Entropie a směr tepelného toku
Druhý zákon termodynamiky zavádí koncept entropie a popisuje nevratnost přírodních procesů. Tento zákon vysvětluje, proč některé procesy probíhají spontánně jedním směrem, ale ne opačným.
Formulace druhého zákona
Existuje několik ekvivalentních formulací druhého zákona:
- Clausiusova formulace: Teplo nemůže samovolně přecházet z chladnějšího tělesa na teplejší.
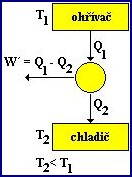
- Kelvinova formulace: Není možné sestrojit periodicky pracující tepelný stroj, který by pouze odebíral teplo z ohřívače a konal ekvivalentní množství práce.
- Entropická formulace: Entropie izolovaného systému vždy roste nebo zůstává konstantní, nikdy neklesá.
Důsledky druhého zákona pro technologii
| Tepelné motory | Nelze dosáhnout 100% účinnosti |
| Chladničky | Vyžadují vnější zdroj energie pro přenos tepla z chladnějšího prostředí do teplejšího |
| Klimatizace | Spotřebovává energii pro vytvoření teplotního rozdílu |
| Tepelná čerpadla | Mají omezenou účinnost závislou na teplotním rozdílu |
| Chemické reakce | Spontánní reakce probíhají ve směru zvyšování celkové entropie |

Třetí zákon termodynamiky: Absolutní nula
Třetí zákon termodynamiky se zabývá chováním systémů blížících se absolutní nule teploty. Tento zákon má důležité implikace pro fyziku a chemii, zejména v oblasti nízkoteplotních jevů.
Nedosažitelnost absolutní nuly
Třetí zákon termodynamiky lze formulovat takto: Je nemožné dosáhnout absolutní nulové teploty konečným počtem kroků.
Důsledky této nedosažitelnosti jsou:
- Nemožnost existence dokonale uspořádaného krystalu
- Limitace v oblasti kvantových výpočtů a supravodivosti
- Fundamentální omezení v chlazení materiálů
Tyto implikace mají významný dopad na výzkum v oblasti fyziky pevných látek, kvantové informatiky a materiálového inženýrství.
Nultý zákon termodynamiky: Teplotní rovnováha
Nultý zákon termodynamiky, ačkoli byl formulován až po ostatních zákonech, je logicky prvním v pořadí. Tento zákon definuje koncept teplotní rovnováhy a umožňuje nám chápat teplotu jako měřitelnou veličinu.
Význam nultého zákona pro měření teploty
Nultý zákon umožňuje konstrukci teploměrů tím, že stanoví:
- Pokud jsou dva systémy v tepelné rovnováze s třetím systémem, jsou v tepelné rovnováze i mezi sebou.
- Toto umožňuje použít standardizovaný referenční systém (teploměr) pro měření teploty různých objektů.
- Bez nultého zákona by koncept teploty jako univerzální veličiny neexistoval.
Aplikace zákonů termodynamiky v praxi
Zákony termodynamiky mají široké uplatnění v každodenním životě i v průmyslu.
Termodynamika v domácnosti
- Fungování ledničky a mrazáku
- Princip vaření a pečení
- Izolace domů pro efektivní vytápění a chlazení
- Ohřev vody v bojleru
- Činnost klimatizace a tepelných čerpadel
Průmyslové využití termodynamických zákonů
| Energetika | Návrh a optimalizace elektráren |
| Automobilový průmysl | Vývoj účinnějších motorů |
| Chemický průmysl | Řízení chemických reakcí a procesů |
| Potravinářství | Konzervace a zpracování potravin |
| Metalurgie | Tavení a zpracování kovů |
| Cryogenika | Zkapalňování plynů a supravodivost |
Závěr
Zákony termodynamiky představují fundamentální principy, které řídí chování energie ve vesmíru. Od každodenních jevů až po nejpokročilejší technologie, tyto zákony formují naše chápání přírodních procesů a umožňují nám vyvíjet efektivnější a udržitelnější technologie. Porozumění těmto zákonům je klíčové nejen pro vědecký pokrok, ale i pro řešení globálních výzev, jako je energetická krize a klimatická změna. S pokračujícím výzkumem v oblastech jako kvantová termodynamika a nerovnovážné systémy se naše chápání těchto principů dále prohlubuje, otevírající nové možnosti pro inovace a technologický rozvoj.